Caveolin‑1(CAV1)是一種乳腺癌抑制基因,人體缺少了它或它發生突變時,就會影響癌細胞的自噬作用和溶酶體功能,增加患上乳腺癌的風險。健康科學學院教授沈漢明發現,可以用CAV1的缺失或突變作為生物指標,指導在臨床上是否適合用自噬抑制劑作為治療乳腺癌的手段。
細胞自噬(Autophagy)是生物進化過程中完整保留的一個重要機制,即細胞通過溶酶體來清除細胞內的損害物質從而讓細胞恢復正常的一個過程。目前已知細胞自噬具有十分重要的生理功能,而且和癌症、神經退行性疾病等許多疾病密切相關。在細胞自噬研究的早期,人們認為細胞自噬會導致細胞自噬性死亡,而沈教授的研究證明,細胞自噬原則上是抵抗飢餓及應急狀態的一個重要的促進細胞生存的機制。
沈教授表示,細胞自噬對癌症是一把雙刃劍:在癌症發生前,增加機體的自噬水平可以起到預防作用;但在已有的腫瘤細胞内,自噬可以促進癌細胞的生存和腫瘤的發生發展。他說:「細胞在飢餓及應急情況下會激活自噬,通過重新利用細胞内的營養元素,例如氨基酸,維持細胞的功能,促進細胞生存。」
來源:《澳大新語》第22期

沈漢明教授曾在新加坡國立大學楊潞齡醫學院從事細胞自噬、氧化損傷、細胞信號傳導等方面的研究20多年,至今在《Autophagy》、《Cell Res》、《Cancer Res》、《Mol Cell》、《Nature Protocol》等SCI期刊發表論文200餘篇,被引用次數超過25,000次。目前在澳大展開關於細胞自噬及溶酶體、線粒體自噬、腫瘤靶向治療等方向的研究。
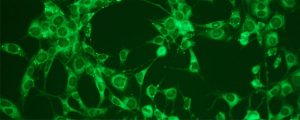
癌細胞在飢餓情況下激活自噬
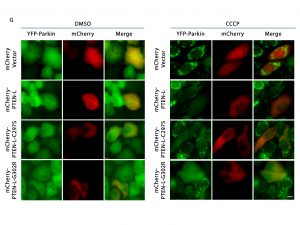
癌細胞進行線粒體自噬
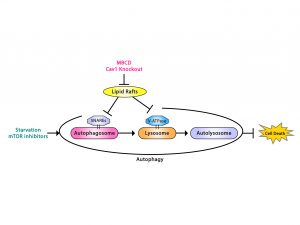
沈漢明教授發現可以用CAV1的缺失或突變作為生物指標,指導在臨床上是否適合用自噬抑制劑作為治療乳腺癌的手段。

