澳門大學健康科學學院副教授郭珩輝及其研究團隊在構建高靈敏型光電化學免疫傳感器方面取得重大進展。研究團隊通過陽離子交換反應,合成出一種先進的納米材料,並且將之應用在基於高效生物傳感系統的高靈敏腫瘤標誌物檢測。該研究在生物傳感器開發和癌症診斷領域備受關注,成果已獲國際知名期刊《生物傳感器和生物電子學》(Biosensors and Bioelectronics)刊登。
腫瘤標誌物指由腫瘤細胞特徵性產生、可用於區別腫瘤細胞和正常細胞的生物學分子,大多存在於患者的組織、血液和體液。檢測出腫瘤標誌物往往有助選擇最佳的臨床治療手段。其中,前列腺特異性抗原(PSA)是一種廣泛用於篩查和診斷前列腺癌的標誌物。科學家近10年來不斷致力提高PSA檢測的靈敏性,從而指導醫生更準確地鑑別良性和惡性腫瘤。郭珩輝教授團隊合成的納米材料正正能用於檢測PSA。
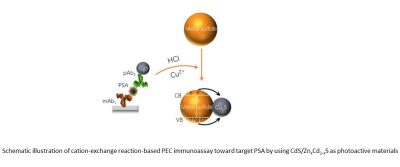
研究團隊根據軟硬酸鹼理論(一項合成中空金屬硫化物的重要理論基礎,英文簡稱HSAB)合成了中空的Cu2-xS納米晶體,並以這種晶體作為光活性材料用於檢測光電流信號,從而檢測PSA。他們首先合成了立體Cu2O晶體,然後通過表面硫化處理和鹽酸蝕刻獲得中空的Cu2-xS納米晶體。他們其後再將硫化銅、磷化氫和其他金屬鹽混合,在不改變原先晶體框架、大小和厚度的情況下,代替其中的銅離子而獲得新的金屬硫化物。這種有趣現象可用HSAB理論解釋,即軟鹼更易與軟酸 (Cu+) 結合並將 Cu+ 從結構中置換。在此基礎上,研究團隊進一步運用該反應系統研發新的PSA光電化學免疫檢測方法。相比純二元硫化物,摻雜多金屬的硫化物(ZnxCd1-xS)有更強的光電流響應,是優良的光電轉化材料,能夠更靈敏地檢測PSA。運用了新的硫化物的檢測方法在1.0 pg/mL~10 ng/mL的範圍內呈線性關係,檢測的最低限度是0.32 pg/mL。
陽離子交換反應的理論可以廣泛用於合成優良的納米材料,以及製造高效的生物傳感系統。這種合成方法簡單,毋需嚴苛反應條件就能進行,有潛力用於大規模製備納米材料。郭教授團隊的研究結果顯示,ZnxCd1-xS中空晶體可以作為光活性材料應用於超靈敏檢測腫瘤標誌物的三明治免疫檢測方法,可望為生物傳感器光活性材料的可控合成和大規模製備提供新思路。
相關論文的通訊作者是郭珩輝,共同第一作者為其博士生郭麗斌和李彬。南京中醫藥大學副教授葛立林曾在研究團隊從事博士後研究,也對該研究作出貢獻。研究項目獲澳門科學技術發展基金資助(檔案編號:0055/2019/A1 和0010/2021/AFJ)。