澳門大學健康科學學院講座教授鄧初夏帶領的研究團隊深入研究三陰性乳腺癌的發生機制以及免疫療法,揭示纖維細胞生長因子受體2(FGFR2)驅動三陰性乳腺癌並建立小鼠模型,成功研發出靶向及免疫聯合療法精準治療三陰性乳腺癌。該研究成果已在國際著名學術期刊《先進科學》(Advanced Sciences)中發表。
乳腺癌為全世界最常見的癌症,其中三陰性乳腺癌被稱為“最難治”的乳腺癌,由於它的侵襲性強,療效差、容易復發轉移,而且死亡率高。縱使現時已有多種的聯合療法用於治療乳腺癌,但三陰性乳腺癌的治療仍然很棘手,因此深入研究驅動三陰性乳腺癌形成的原因及靶向治療迫在眉睫。
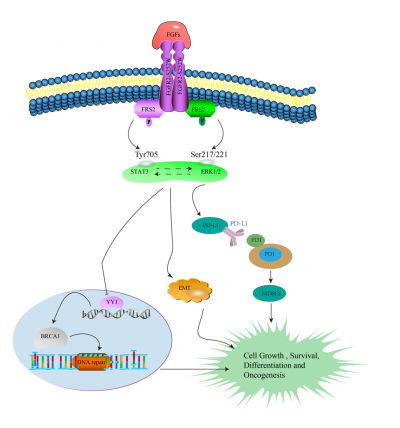
常見的乳腺腫瘤有四種不同的分子分型,分別是Luminal A型、Luminal B型、HER-2過表達型和三陰性型。FGFR2是介導約22種成纖維細胞生長因數(FGFs)信號的四種膜結合受體酪氨酸激酶(RTKs) 之一。FGFR2的基因突變可以啟動FGFR2的下游信號通路,例如,PI3K-AKT, MAPK,及mTOR信號通路等。團隊利用Cre/Loxp系統在乳腺組織中特異性的啟動FGFR2,隨後通過多種技術手段分析小鼠乳腺的發育狀況,經過一年至一年半時間逐漸發現小鼠乳腺有腫瘤發生,證實了FGFR2轉基因小鼠可以驅動乳腺腫瘤形成。利用基因組測序和免疫染色系統分析FGFR2腫瘤的資訊,發現約有50%的腫瘤都是三陰性型,因此利用此方法建立了三陰性乳腺癌的小鼠模型,並以早期乳腺基因組資訊為線索,揭示FGFR2腫瘤的發生可能與上皮細胞的分化、增殖、炎症反應、MAPK級聯反應、趨化因數等過程相關。同時,進一步在體內體外實驗驗證發現FGFR2-S252W突變啟動FGFR2/STAT3/MAPK通路,促進三陰性乳腺癌的形成;利用抑制轉錄因數YY1來調控BRCA1的功能;促進炎症因數的釋放,調控免疫檢查點PD-L1的表達。研究團隊最後利用三維腫瘤切片技術,成功開發靶向FGFR2聯合免疫療法精準治療三陰性乳腺癌。
此次研究的通訊作者為鄧初夏,其博士生雷海鵬為第一作者,該研究得到副教授徐曉玲、副教授(臨床醫生)姚志成、助理教授陳強、研究助理教授 Mi-Hye Lee、苗凱和孫恒對該研究作出重要貢獻。此項研究由國家教育部澳門大學精準腫瘤學前沿科學中心,國家自然科學基金(NSFC: 82030094)及澳門科學技術發展基金資助(檔案編號:FDCT-0048/2019/A1 和 FDCT-0011/2019/AKP)。全文可瀏覽:https://doi.org/10.1002/advs.202100974。