澳門大學健康科學學院助理教授代雲路帶領的研究團隊製成基於多酚與金屬離子相結合的納米藥物,其在血液環境中結構穩定,循環時間長,可有效積累於腫瘤組織,實現了通過調節腫瘤微環境來提高聲動力療效,能有效抑制腫瘤的生長及轉移。此新型治療策略已刊登於國際著名學術期刊《ACS Nano》。
多酚廣泛存在於自然界的各種植物中,是植物體內的重要有機成分。其獨特的酚羥基結構及物理特性使其具有特定的生理功效,可應用於預防退行性疾病及對抗癌症等。多酚的酚羥基與金屬離子可以通過配位螯合作用形成可逆的三維網絡結構,該共價偶聯性質賦予多酚優秀的功能化修飾特性,實現不同藥物的承載和靶向運送。代雲路的團隊利用獨特的金屬-多酚配位生物材料設計理念,進行天然多酚、多酚衍生物的模塊化合成和製備。
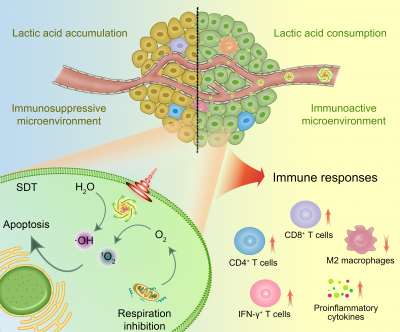
在此研究中,團隊成員通過化學方法將卟吩與多酚相結合,合成具有聲敏性質的多酚衍生物,並將其與具備腫瘤微環境調節作用的乳酸氧化酶和阿托伐醌相結合,進一步與鐵離子配位,獲得納米化多酚藥物。此納米製劑體積小,直徑約100納米,在血液環境中結構穩定,循環時間長,能有效積累於腫瘤組織。利用超聲輻照此納米藥物可誘發產生大量活性氧,同時通過逆轉免疫抑制酸性腫瘤微環境,造成腫瘤細胞損傷。此納米藥物可有效引起機體對腫瘤的免疫應答,誘導大量抗腫瘤細胞因數的釋放及免疫細胞在腫瘤組織的浸潤,有效抑制腫瘤生長及轉移。
是次研究的通訊作者為代雲路,其博士生張展為第一作者。三位博士後李蓓、謝麗斯、李傑及三位博士生桑瑋、田浩、王國浩亦作出重要的貢獻。此項研究由澳門科學技術發展基金(檔案編號:0109/2018/A3 和0011/019/AKP)、澳門大學(檔案編號:SRG2018-00130-FHS)和深圳-香港-澳門科技項目資助(檔案編號:SGDX20201103093600004)。研究文章全文可瀏覽:https://pubs.acs.org/doi/10.1021/acsnano.1c08026