澳門大學健康科學學院副教授劉子銘帶領的團隊在抗癌藥物篩選技術上取得了重大進展。該研究利用類脂褐素紅色自發螢光,提早預測細胞凋亡進程,並可以無創地持續監測3D腫瘤活體切片的藥效反應動態,以及識別斑馬魚胚胎發育中的細胞凋亡。同時,通過對類脂褐素的螢光壽命分析可進一步區分細胞壞死與凋亡。此研究確立了類脂褐素紅色自發螢光能作為細胞死亡的標誌物,拓展藥效學的信息維度,為類器官替身試藥的研究與應用提供了新視角。相關研究成果在生物學領域備受矚目,並已獲國際知名期刊《氧化還原生物學》(Redox Biology)以論文形式刊登。
細胞凋亡是一種經常發生且受到嚴格調控的生物化學過程,用於維持生物組織穩態,細胞凋亡的失調可能導致不受控制的增殖和惡性腫瘤。當前癌症的化療藥物或細胞治療,是以觸發癌細胞凋亡途徑來達成治療效果。隨著對細胞死亡機制的深入了解,一些生化特徵已被用於檢測細胞死亡,然而這些方法需要對組織進行固定和染色,這限制了時序評估的可能性。為了使藥效學和細胞凋亡反應可視化,科學家們設計了活細胞染色探針,所有這些報告分析都依賴於外源試劑、合成納米探針或複雜的基因轉染方案,這外部措施會改變待測細胞的生理狀態。細胞中的內源性螢光團,如NADH、核黃素等,可以實現細胞衰亡的快速和免標記評估,然而這些代謝螢光團並非細胞衰亡所特有,很容易受到其他代謝活動的影響。因此,開發一種利用內源性螢光團且可以特異性標記細胞死亡進程的檢測方法,對揭示藥效動力、測試藥物敏感性具有重大的意義。
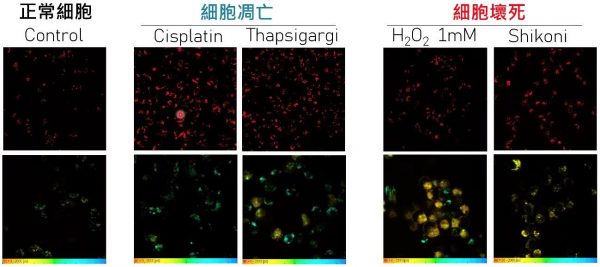
脂褐素是一種具有自發螢光特性的棕黃色素顆粒,在組織衰老過程中會在細胞中積累。過去,脂褐素被廣泛用於指示視網膜、神經元、心肌和人間充質基質細胞的衰老退化。研究團隊利用藥物誘導細胞死亡,並使用雙光子顯微成像技術觀測類脂褐素紅色自發螢光強度,結果發現凋亡和壞死細胞的溶酶體類脂褐素紅色螢光,較正常細胞顯著增強,同時根據自發螢光壽命分析,進一步區分細胞的凋亡和壞死。接著團隊將此免標記細胞死亡檢測技術,成功的應用在癌症精準醫療的替身試藥體系,包括微型腫瘤球體、患者來源類器官 (PDO)、以及保有免疫細胞的三維腫瘤切片培養 (3D-TSC) 模型。通過連續的藥效學監測,此項技術可以優化藥敏性評估,克服不同遺傳背景和組織異質性所帶來的個體藥效差異,提高藥物篩選的通量。
此次研究的通訊作者為劉子銘、澳大健康科學學院院長鄧初夏、教授羅茜及副教授李子安,博士生閆映寒及邢富強共同為第一作者。澳大健康科學學院的研究助理曹家悅,博士生胡益靈等也對這項研究做出了重要的貢獻。該項目由澳門特別行政區科學技術發展基金(檔案編號:122/2016/A3, 018/2017/A1, 0011/2019/AKP, 0002/2021/AKP; 0007/2021/AKP, 0120/2020/A3, 0026/2021/A)和澳門大學(檔案編號:MYRG2018-00070-FHS)資助。研究文章完整版本可瀏覽https://www.sciencedirect.com/science/article/pii/S2213231722003500?via%3Dihub。